اسید سولفوریک (H₂SO₄)، که به نام «جوهر گوگرد» نیز شناخته میشود، یکی از اسیدهای معدنی بسیار قوی و پرکاربرد در صنایع و آزمایشگاهها است. این اسید قوی با خاصیت خورندگی شدید و واکنشپذیری بالا نقش کلیدی در تولید کودهای شیمیایی، فرآوری فلزات، صنایع پتروشیمی، باتریهای اسیدی و واکنشهای شیمیایی آزمایشگاهی ایفا میکند. اگرچه اسید سولفوریک بهطور خالص در طبیعت یافت نمیشود، منابع گوگردی و فرایندهای طبیعی میتوانند منجر به تولید سولفوریک اسید یا یونهای سولفات شوند. در عین حال، تماس مستقیم یا استنشاق این اسید برای انسان بسیار خطرناک است و رعایت نکات ایمنی دقیق هنگام کار با آن الزامی است. این متن ضمن معرفی ویژگیها و منابع طبیعی سولفوریک اسید، خطرات، کاربردها و روشهای اندازهگیری آن را بررسی کرده و اهمیت رعایت ایمنی در محیطهای صنعتی و آزمایشگاهی را برجسته میکند.
اسید سولفوریک چیست؟
سولفوریک اسید که با نام رایج «جوهر گوگرد» نیز شناخته میشود، یک اسید معدنی قوی و بسیار خورنده با فرمول شیمیایی H₂SO₄ است. این ترکیب شیمیایی بیرنگ تا کمی زرد کمرنگ بوده و در آب بسیار محلول است و هنگام حل شدن در آب گرمای زیادی تولید میکند. سولفوریک اسید کاربردهای گستردهای در صنایع مختلف دارد، از جمله تولید کودهای شیمیایی، تصفیه فلزات، صنایع پتروشیمی، باتریهای اسیدی و واکنشهای شیمیایی آزمایشگاهی. به دلیل خاصیت خورندگی شدید، تماس آن با پوست یا استنشاق بخارات آن بسیار خطرناک است و نیازمند رعایت نکات ایمنی دقیق است.
منابع طبیعی سولفوریک اسید
اسید سولفوریک (H₂SO₄) بهطور طبیعی به صورت خالص در محیط زیست یافت نمیشود، اما منابع و ترکیبات طبیعیای وجود دارند که در اثر فرایندهای طبیعی میتوانند منجر به تولید سولفوریک اسید یا یونهای سولفات شوند. مهمترین منابع طبیعی عبارتند از:
- گوگرد معدنی: ذخایر گوگرد طبیعی در زمین، مانند گوگرد عنصری یا ترکیبات سولفیدی (مثل پیریت FeS₂)، در اثر اکسید شدن میتوانند به تولید سولفوریک اسید منجر شوند.
- آتشفشانها: گازهای گوگردی منتشر شده از فعالیتهای آتشفشانی، مانند دیاکسید گوگرد (SO₂)، در تماس با رطوبت جو و واکنش با اکسیژن میتوانند به سولفوریک اسید تبدیل شوند.
- باران اسیدی طبیعی: بارش بارانهایی که شامل SO₂ و دیگر ترکیبات گوگردی هستند، در محیط مرطوب با آب واکنش داده و سولفوریک اسید ضعیف ایجاد میکنند.
- تجزیه مواد آلی گوگرددار: فرآیندهای میکروبی و شیمیایی در خاک و رسوبات که شامل ترکیبات گوگرددار هستند نیز میتوانند سولفوریک اسید تولید کنند، هرچند با غلظت کم.
بنابراین، اگرچه اسید سولفوریک به شکل خالص به صورت طبیعی وجود ندارد، اما منابع گوگردی و فرآیندهای اکسیداسیون طبیعی گوگرد، پایه تشکیل سولفوریک اسید در طبیعت هستند.
سولفوریک اسید در بدن
اسید سولفوریک (H₂SO₄) بهطور طبیعی در بدن انسان به عنوان بخشی از اسید معده (هیدروکلریک اسید و ترکیبات گوگردی) یافت نمیشود و وارد کردن آن از خارج به بدن بسیار خطرناک است. تماس یا بلع این اسید موجب سوختگی شدید دهان، گلو و معده، درد شدید و آسیب جدی به دستگاه گوارش میشود و میتواند تهدیدکننده زندگی باشد. بدن انسان توانایی خنثی کردن یا دفع این اسید قوی را ندارد و حتی مقدار کم آن میتواند باعث آسیب بافتی جدی شود. بنابراین، اسید سولفوریک هیچ کاربرد داخلی یا تغذیهای ندارد و تنها استفاده آن در محیطهای کنترلشده صنعتی یا آزمایشگاهی مجاز است.
خطرات سولفوریک اسید چیست؟
سولفوریک اسید (H₂SO₄) یک ماده شیمیایی بسیار خورنده و خطرناک است و تماس با آن میتواند اثرات جدی بر سلامت داشته باشد. مهمترین خطرات آن عبارتند از:
- خطر برای پوست و چشم: تماس مستقیم باعث سوختگی شدید پوست، تحریک، تاول و آسیب دائمی به چشمها میشود و حتی ممکن است باعث کوری شود.
- خطر استنشاق: بخارات یا ذرات اسید میتوانند باعث تحریک شدید مجاری تنفسی، سرفه، تنگی نفس، التهاب ریه و در موارد شدید آسیب دائمی به ریهها شوند.
- خطر بلعیدن: بلعیدن سولفوریک اسید موجب سوختگی دهان، گلو و معده، درد شدید و آسیب جدی به دستگاه گوارش میشود و میتواند تهدیدکننده زندگی باشد.
- خطر واکنشهای شیمیایی: تماس با مواد آلی، بازها یا فلزات میتواند باعث واکنش شدید، تولید حرارت، جرقه یا گازهای سمی شود.
- خطر محیط زیستی: ریختن سولفوریک اسید در محیط زیست موجب اسیدی شدن خاک و آبها و آسیب به گیاهان و موجودات زنده میشود.
استفاده از دستکش، عینک ایمنی، روپوش آزمایشگاهی و تهویه مناسب هنگام کار با سولفوریک اسید الزامی است تا از بروز این خطرات جلوگیری شود.
نکات ایمنی هنگام کار با سوفوریک اسید
البته! هنگام کار با اسید سولفوریک (H₂SO₄)، به دلیل خاصیت بسیار خورنده و واکنشپذیری شدید آن، رعایت نکات ایمنی بسیار ضروری است. در ادامه مهمترین نکات را بهصورت دستهبندی شده آوردهام:
تجهیزات حفاظت فردی (PPE)
- استفاده از دستکش مقاوم به مواد شیمیایی (مانند نیتریل یا لاتکس ضخیم).
- پوشیدن عینک ایمنی یا شیلد صورت برای محافظت از چشمها و صورت.
- لباس آزمایشگاهی مقاوم، با آستین بلند و ترجیحاً پیشبند مقاوم به اسید.
- در صورت نیاز، استفاده از ماسک یا تهویه مناسب برای جلوگیری از استنشاق بخارات.
نحوه جابجایی و نگهداری
- همیشه بطری یا ظرف اسید را محکم نگه دارید و از افتادن یا تکان شدید جلوگیری کنید.
- هرگز آب را به اسید اضافه نکنید؛ همیشه اسید را به آرامی در آب بریزید تا واکنش شدید و پاشیدن جلوگیری شود.
- اسید را در ظرف شیشهای یا پلیاتیلنی مقاوم و در محیط خنک، خشک و تهویهدار نگهداری کنید.
- از نگهداری اسید در نزدیکی مواد قابل اشتعال یا بازها اجتناب کنید.
اقدامات در صورت تماس
- تماس با پوست: فوراً با آب زیاد شستشو دهید و در صورت سوختگی شدید به پزشک مراجعه کنید.
- تماس با چشم: حداقل ۱۵ دقیقه با آب شستشو دهید و سریعاً به پزشک مراجعه کنید.
- استنشاق بخار: فرد را به هوای تازه منتقل کنید و در صورت مشکلات تنفسی، کمک پزشکی دریافت کنید.
- بلعیدن: هیچگاه باعث استفراغ نکنید و فوراً به مرکز درمانی مراجعه کنید.
اقدامات پیشگیرانه و ایمنی عمومی
- محل کار باید تهویه مناسب داشته باشد.
- آتشنشانی و تجهیزات اضطراری شامل دوش اضطراری و چشمشوی نزدیک محل کار در دسترس باشد.
- ظروف اسید را بهدرستی برچسبگذاری کنید و دسترسی افراد غیرمجاز را محدود کنید.
- با اسید، به آرامی و با دقت کار کنید و از هرگونه رفتار عجولانه یا بازیگوشانه پرهیز کنید.
کاربرد اسید سولفوریک
اسید سولفوریک (H₂SO₄) یکی از پرکاربردترین و مهمترین اسیدهای معدنی در جهان است که نقش کلیدی در صنایع، فرآوری فلزات و فعالیتهای آزمایشگاهی ایفا میکند. به دلیل خاصیت خورندگی قوی و واکنشپذیری بالای آن، استفاده از این اسید در زمینههای مختلف نیازمند کنترل دقیق و رعایت نکات ایمنی است. در متن پیش رو، به بررسی کاربردهای اسید سولفوریک در سه حوزه اصلی پرداخته شده است: صنایع پتروشیمی، تصفیه و فرآوری فلزات و کاربردهای آزمایشگاهی، که هر یک اهمیت ویژهای در بهبود کیفیت محصولات و افزایش بهرهوری فرآیندها دارند.
اسید سولفوریک در صنایع پتروشیمی
در صنایع پتروشیمی، اسید سولفوریک (H₂SO₄) بهعنوان یک کاتالیزور و ماده شیمیایی پایه کاربرد گسترده دارد. این اسید در تولید انواع ترکیبات آلی مانند الکلها، اترها، سولفوناتها و اسیدهای آلی نقش مهمی ایفا میکند و به افزایش راندمان واکنشهای شیمیایی کمک میکند. همچنین در فرآیندهای استخراج و تصفیه محصولات پتروشیمی، مانند تولید بنزین و ترکیبات گوگرددار، استفاده میشود. کاربرد کنترلشده اسید سولفوریک در این صنایع موجب بهبود کیفیت محصولات، افزایش بهرهوری و کاهش ناخالصیها میشود، اما به دلیل خورندگی شدید آن، نگهداری و استفاده از آن نیازمند تجهیزات و ایمنی دقیق است.
اسید سولفوریک برای تصفیه و فرآوری فلزات
در تصفیه و فرآوری فلزات، اسید سولفوریک (H₂SO₄) نقش مهمی بهعنوان عامل اسیدی و پاککننده سطح فلزات ایفا میکند. این اسید برای زدودن اکسیدها، زنگزدگی و ناخالصیهای سطحی فلزات قبل از عملیات آبکاری، لحیمکاری یا سایر فرآیندهای صنعتی استفاده میشود. همچنین در استخراج فلزات از سنگ معدنها، مانند روی، مس و آهن، بهعنوان محلول اسیدی برای حل کردن و جداسازی فلزات به کار میرود. استفاده کنترلشده از اسید سولفوریک باعث بهبود کیفیت سطح فلزات، افزایش چسبندگی پوششها و افزایش بهرهوری فرآیندهای فلزی میشود، در حالی که رعایت نکات ایمنی برای جلوگیری از خورندگی و آسیب به تجهیزات و نیروی انسانی ضروری است.
کاربردهای آزمایشگاهی اسید سولفوریک
در محیطهای آزمایشگاهی، اسید سولفوریک (H₂SO₄) یکی از مواد شیمیایی پرکاربرد است و نقش مهمی در انجام واکنشهای شیمیایی و سنتز ترکیبات دارد. این اسید بهعنوان عامل خشککن، کاتالیزور در واکنشهای شیمیایی و عامل اسیدی برای تنظیم pH استفاده میشود. همچنین در آنالیزهای شیمیایی، مانند تعیین مقادیر فسفر و نیتروژن، و در آمادهسازی نمونهها برای تجزیه و استخراج مواد مختلف کاربرد دارد. استفاده از اسید سولفوریک در آزمایشگاه نیازمند رعایت دقیق نکات ایمنی، استفاده از تجهیزات محافظتی و تهویه مناسب است، زیرا تماس مستقیم با پوست، چشم یا استنشاق بخارات آن بسیار خطرناک است.
روش های اندازه گیری سولفوریک اسید
اندازهگیری سولفوریک اسید (H₂SO₄) در محیطهای صنعتی، آزمایشگاهی و محیط زیست به روشهای مختلفی انجام میشود که هر کدام بسته به دقت مورد نیاز، حجم نمونه و شرایط کاری انتخاب میشوند. مهمترین روشها عبارتند از:
- تیتراسیون اسید-باز: یکی از رایجترین روشها برای تعیین غلظت سولفوریک اسید در محلولها است که با استفاده از باز استاندارد مانند سدیم هیدروکسید و یک نشانگر مناسب انجام میشود.
- اندازهگیری با دراگر تیوبها: تیوبهای مخصوص مانند Dräger کد 6728781 امکان پایش بخارات سولفوریک اسید در هوا را فراهم میکنند و برای کنترل ایمنی محیط کاربرد دارند.
- روش اسپکتروفوتومتری: این روش بر اساس جذب نور در طول موج مشخص توسط یونهای سولفات انجام میشود و برای نمونههای رقیق و محلولهای صنعتی کاربرد دارد.
- کروماتوگرافی یونی (Ion Chromatography): روش دقیق و حساس برای تعیین غلظت یونهای سولفات در نمونههای آب، خاک یا محلولهای صنعتی است.
- الکتروشیمیایی: استفاده از سنسورها و الکترودهای خاص برای اندازهگیری مستقیم غلظت اسید در محلولها یا بخارات.
دراگر تیوب سولفوریک اسید Drager کد 6728781
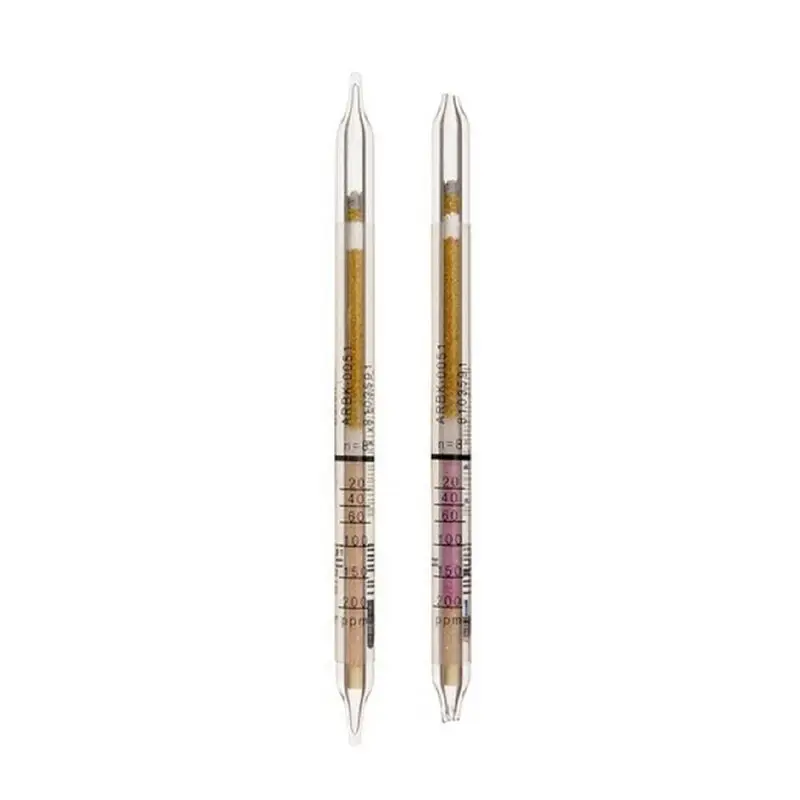
دراگر تیوب سولفوریک اسید Dräger کد 6728781 یک ابزار تخصصی برای اندازهگیری و پایش دقیق غلظت بخارات سولفوریک اسید در محیطهای صنعتی و آزمایشگاهی است. این تیوبها با طراحی حساس و استاندارد، امکان شناسایی و کنترل سطح بخارات خورنده H₂SO₄ را فراهم میکنند و به افزایش ایمنی کارکنان و کاهش خطرات ناشی از تماس یا استنشاق این اسید کمک میکنند. استفاده از دراگر تیوب سولفوریک اسید Dräger کد 6728781 به واحدهای صنعتی، آزمایشگاهها و مراکز پتروشیمی اجازه میدهد تا بهصورت مداوم وضعیت محیط را پایش کنند و اقدامات پیشگیرانه مناسب را انجام دهند.
نتیجهگیری
اسید سولفوریک (H₂SO₄) با ویژگیهای خورندگی شدید و کاربردهای گسترده در صنایع پتروشیمی، تصفیه فلزات و آزمایشگاهها، یکی از مواد شیمیایی حیاتی و در عین حال خطرناک محسوب میشود. این اسید بهطور طبیعی در محیط زیست به شکل خالص یافت نمیشود، اما منابع گوگردی و فرآیندهای اکسیداسیون طبیعی پایه تولید آن را فراهم میکنند. تماس مستقیم یا استنشاق سولفوریک اسید میتواند خطرات جدی برای سلامت انسان و محیط زیست به همراه داشته باشد، بنابراین رعایت نکات ایمنی و استفاده از تجهیزات حفاظتی الزامی است. علاوه بر کاربردهای صنعتی و آزمایشگاهی، روشهای مختلفی برای اندازهگیری و پایش غلظت این اسید، از جمله تیتراسیون، اسپکتروفوتومتری و دراگر تیوبهای تخصصی، وجود دارد که به کنترل ایمنی و کاهش خطرات کمک میکنند. بهطور کلی، استفاده مسئولانه و کنترلشده از سولفوریک اسید، هم به بهرهوری فرآیندها و کیفیت محصولات کمک میکند و هم سلامت افراد و محیط زیست را حفظ میکند.










